职位推荐
- 珍格医疗-临床销售 15001-20000
- 地奥制药-医药代表 6001-8000
- 普利德医疗-医疗设备销售经理 面议
- 大唐-兼职招商经理 面议
- 景德中药-直营经理 6001-8000
- 安邦医药-省区招商经理 8001-10000
- 恒瑞医药-医药信息沟通专员 6001-8000
- 黄河中药-学术讲师 8001-10000
发布日期:2019-09-12 浏览次数:464
9月12日,恒瑞医药卡瑞利珠单抗单药二线治疗晚期食管鳞癌、卡瑞利珠单抗联合培美曲塞加卡铂一线治疗晚期或转移性非鳞癌非小细胞肺癌的上市申请获得国家药品监督管理局受理。
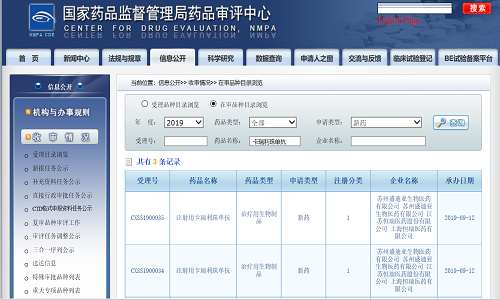
恒瑞医药卡瑞利珠单抗联合培美曲塞加卡铂与培美曲塞加卡铂一线治疗晚期或转移性非鳞癌非小细胞肺癌患者的随机对照多中心III期临床研究由同济大学医学院附属上海市肺科医院周彩存教授担任主要研究者,牵头52家中心负责完成。近日,该项研究全体受试人群的主要终点-IRC评估的无进展生存期(PFS)达到方案预设的期中分析优效判定标准,且安全性可接受。研究结果表明,对于一线的晚期或转移性非鳞癌非小细胞肺癌患者,接受卡瑞利珠单抗联合培美曲塞加卡铂治疗对比培美曲塞加卡铂一线治疗,可显著延长患者的无进展生存期。卡瑞利珠单抗单药二线治疗晚期食管鳞癌的随机、开放、化疗药对照、多中心III期临床研究已于2019年7月达到主要研究终点。
注射用卡瑞利珠单抗是恒瑞医药自主研发并具有知识产权的人源化PD-1单克隆抗体,已于2019年5月获批上市。目前,除已获批的复发/难治性霍奇金淋巴瘤适应症外,已有肝细胞癌、晚期食管鳞癌、晚期或转移性非鳞癌非小细胞肺癌等 3 个新适应症申报上市,其中,肝细胞癌适应症基于II期临床试验获得的疗效和安全性数据被国家药品监督管理局纳入拟优先审评。与此同时,恒瑞医药正在中国开展评估卡瑞利珠单抗单药或联合不同的治疗手段的32项研究,其中,卡瑞利珠单抗联合阿帕替尼一线治疗晚期肝细胞癌III期临床研究正在中国、美国等地同步开展。
300多万优质简历
17年行业积淀
2万多家合作名企业

微信扫一扫 使用小程序

