职位推荐
- 珍格医疗-临床销售 15001-20000
- 地奥制药-医药代表 6001-8000
- 普利德医疗-医疗设备销售经理 面议
- 大唐-兼职招商经理 面议
- 景德中药-直营经理 6001-8000
- 安邦医药-省区招商经理 8001-10000
- 恒瑞医药-医药信息沟通专员 6001-8000
- 黄河中药-学术讲师 8001-10000
发布日期:2020-08-10 浏览次数:111
一、公司概述
汇宇制药成立于2010年,主要从事抗肿瘤和注射剂药物的研发、生产和销售。公司生产与质量总部位于内江市国家级经济技术开发区,研发中心坐落于成都市天府国际生物城。
二、公司简介
汇宇制药是一家研发驱动的综合制药企业,主要从事抗肿瘤和注射剂药物的研发、生产和销售。
公司的研发团队以经验丰富的海归博士为核心,截止2020年底,公司研发人员将近400人,占公司总人数的近40%,在化学原料药、化学普通注射剂和复杂注射剂等方面有丰富的研发经验,同时积极推进抗肿瘤领域的小分子创新药和生物大分子创新药的研发。截止2021年8月,公司在研项目超过80个,包含10个一类创新药项目,管线以肿瘤及相关领域为主,同时逐步覆盖其它领域。

在海外,汇宇制药2014年首次通过英国GMP认证,2015年7月全资子公司英国海玥药业通过欧盟药品放行资质认证,同年自主品牌抗肿瘤注射剂在欧盟实现规模化销售。公司自有或授权合作方持有海外批件超过100件,在近90个国家签订了合作协议,覆盖6大洲。截止2021年8月,汇宇在英国有11个一线抗肿瘤及相关领域的注射剂获得上市批准,并在海外超过1000家医疗机构上市销售。
在国内,2017年注射用培美曲塞二钠视同通过一致性评价,次年中标国家集采,在国内开始大规模销售,覆盖了超过2000家等级医院。截止2021年8月,公司有注射用培美曲塞二钠、多西他赛注射液、注射用阿扎胞苷、紫杉醇注射液、奥沙利铂注射液、注射用盐酸苯达莫司汀、伊立替康注射液等7个药品在中国获批上市,均视同通过注射剂一致性评价,且汇宇制药都是在同品种中前三家过评企业。

三、荣誉及奖项
(1)2016 年,荣获四川省院士(专家)工作站;
(2)2016 年,荣获博士后创新实践基地;
(3)2018 年,荣获四川省工程实验室;
(4)2019 年,荣获四川省“绿色工厂”;
(5)2019年,荣获四川省“引才引智基地”;
(6)2019年,荣获四川省“高成长型中小企业”。
四、企业文化
1、愿景
成为一家受人尊敬的国际化制药企业
2、企业使命
为全球患者提供疗效确切、质量精湛、价格合理的药品,让癌症成为一种可以控制的慢性病
3、核心价值观
关爱生命,追求卓越,简单诚信
五、发展历程
2010年,汇宇制药注册成立
2011年,英国子公司海玥注册
2013年,内江中欧共线生产基地启用
2014年,先后通过英国和中国GMP认证;
2015年,英国海玥取得欧盟药品放行资质认证并在英国上市销售
2016年,四川省院士(专家)工作站、四川省博士后创新实践基地
2017年,培美曲塞获批视同通过一致性评价的注射剂;
2018年,注射用培美曲塞中标集采,承担三项国家重大新药创制重大科技专项
2019年,多西他赛注射液获批通过一致性评价、在英国荣获最佳抗肿瘤注射剂奖、注射用阿扎胞苷首仿通过一致性评价
2020年,注射用阿扎胞苷中标第三批国家集采、递交科创板IPO申请、汇宇欧盟标准注射剂产业化基地(二期)项目启动、汇宇创新药物研究院建设项目奠基
六、研发实力
1、核心研发团队
经过多年的发展与培养,汇宇制药已汇聚一批优秀的技术、管理和销售人才,形成了一支专业背景突出、研发经验丰富的研发团队。截至2020年12月末,公司拥有员工999人,其中博士和硕士共计122人,大学本科学历人员499人,大学及大学以上人员占总人数的62.16%,已形成较为科学的人才培养梯队。截至2020年12月末,公司研发团队将近400人,占公司总人数的近40%。




2、研发平台
汇宇制药的先进技术及技术平台包括化学仿制注射剂一致性评价技术平台、复杂注射剂生产与质量控制技术平台、原料药生产质量控制技术平台(包括手性药物研发平台、结晶纯化平台、制备纯化平台),以及符合欧盟标准的生产质量管理体系和高效的国际注册体系。
受益于上述研发平台及技术,公司在国内已经申报审批的药品包括普乐沙福注射液等多个品种。截止2021年8月,公司在国际市场,公司自主获批和授权获批的产品批件总数超过100个。在国内市场,公司为注射用阿扎胞苷产品视同通过一致性评价的国内两家首仿企业之一。注射用培美曲塞二钠独家中选“4+7”带量采购,并与原研药厂家共同中选联盟地区带量采购,注射用阿扎胞苷已于2020年8月中选国家第三批药品集中采购。注射用培美曲塞二钠、多西他赛注射液、唑来膦酸注射液等品种已经实现大规模销售并成为公司主要利润来源。
七、产品目录
国内已上市产品:注射用培美曲塞二钠、多西他赛注射液、注射用阿扎胞苷、紫杉醇注射液、奥沙利铂注射液、注射用盐酸苯达莫司汀、伊立替康注射液。
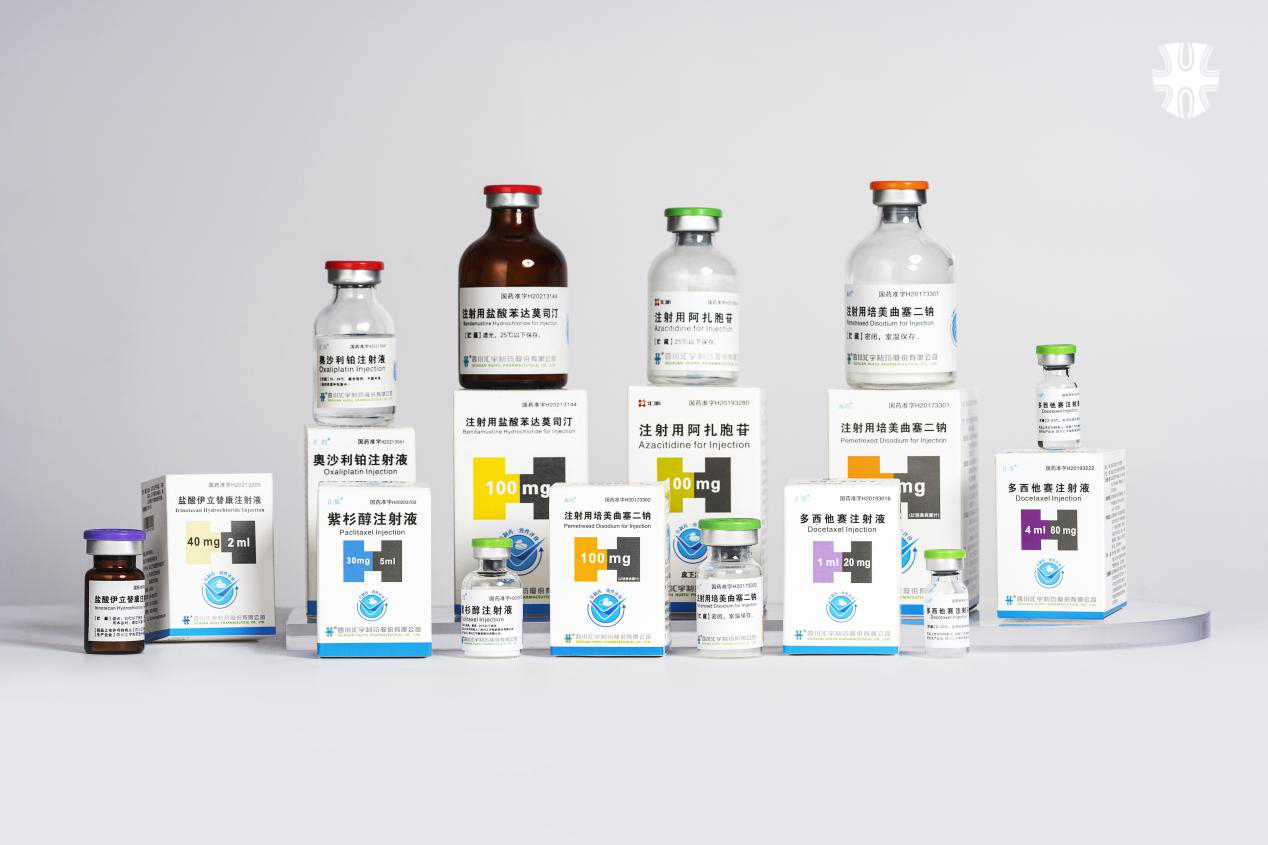
六种药物提交注册审批:注射用硼替唑米、普乐沙福注射液、醋酸奥曲肽注射液、盐酸帕洛诺司琼注射液、左乙拉西坦注射用浓溶液、丙戊酸钠注射液。
八、产品质量
汇宇制药生产及质量中心,位于内江市国家级经济技术开发区内,占地160亩,包含多个生产车间、质量研究和检测中心、行政办公区等多个功能区;其中,质量研究和检测中心,占地近3000平米,50多间实验室,全流程管控产品质量;基地多次通过中国、英国GMP认证;




质量源自严苛的质量理念
坚持“患者第一,质量至上”,严格把控流入市场的每一瓶药,为每一位患者保驾护航,让生命更加有尊严的延续,汇宇制药始终秉承“质量至上”的核心要求,将药品质量风险管控贯穿于药品研发、技术转移、商业化生产的整个产品生命周期。
从生产过程监控到产品上市放行,始终以高标准、最真实的数据对药品质量做出最准确的评价,确保生产和检测过程的每一步经过严格的验证程序,从而保障稳定的产品质量。
质量源于严谨管理体系
汇宇制药依据中国GMP、欧盟GMP、美国FDA法规要求,建立了严谨的质量管理体系,多次通过了中国的GMP认证和英国药监机构(MHRA)的GMP认证。
在汇宇制药,涉及产品质量的要求,皆采用最严格的标准,确保每一瓶、每一滴都高于中国、美国、欧洲药典的质量标准。
质量源自顶级设备保障
公司生产线按德国美施威尔公司的设计理念,引进国际先进设备。公司生产线采用全密闭隔离器(ISOLATOR)、封闭式隔离器(CRABS)、VHP灭菌、冻干机自动进出料、在线称重等国际前沿技术,世界领先水平的全自动智能生产装备,杜绝了人为干扰造成产品污染的风险,生产工艺实现全流程低温生产技术,降低了杂质产生和活性物质降解的风险。
九、子公司
1、英国海玥
英国海玥,全称SEACROSS PHARMACEUTICALS LTD
2、爱尔兰海玥
爱尔兰海玥,全称SEACROSS PHARMA (EUROPE) LIMITED
3、四川泽宇
四川泽宇,全称四川泽宇药业有限公司
4、汇宇海玥
汇宇海玥,全称四川汇宇海玥医药科技有限公司
5、药业科技
药业科技,全称四川汇宇药业科技有限公司
6、汇宇汇昕
汇宇汇昕,全称四川汇宇汇昕医药科技有限公司
7、汇宇生物
汇宇生物,全称成都汇宇生物技术有限公司
8、海玥药业
海玥药业,全称海玥药业(四川)有限公司
9、药物研究
药物研究,全称四川汇宇药物研究有限公司
300多万优质简历
17年行业积淀
2万多家合作名企业

微信扫一扫 使用小程序

