职位推荐
- 珍格医疗-临床销售 15001-20000
- 地奥制药-医药代表 6001-8000
- 普利德医疗-医疗设备销售经理 面议
- 大唐-兼职招商经理 面议
- 景德中药-直营经理 6001-8000
- 安邦医药-省区招商经理 8001-10000
- 恒瑞医药-医药信息沟通专员 6001-8000
- 黄河中药-学术讲师 8001-10000
发布日期:2025-04-21 浏览次数:76
近日,北京大学肿瘤医院沈琳、张小田教授牵头开展的“卡瑞利珠单抗联合阿帕替尼和SOX一线治疗产甲胎蛋白胃癌研究(CAP 06)”发表于《自然》子刊、国际知名医学期刊《信号转导与靶向治疗》(Signal Transduction and Targeted Therapy,简称STTT,IF:40.8)1。该研究曾在2024年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO GI)上首次公布数据2。结果表明,恒瑞创新药卡瑞利珠单抗联合阿帕替尼(“双艾”组合)和SOX(奥沙利铂+替吉奥)一线治疗产甲胎蛋白(AFP)胃癌显示出有希望的抗肿瘤活性,安全性可接受。客观缓解率(ORR)达到66.7%,疾病控制率(DCR)为88.9%,中位无进展生存期(PFS)为7.8个月,中位总生存期(OS)为18.0个月。
CAP 06研究发表于STTT
01研究背景
AFP是主要由胎儿的肝脏和卵黄囊产生的一种糖蛋白。出生后其合成受到抑制,血浆浓度稳定于0~20ng/ml。但AFP在恶性肿瘤血浆浓度中明显升高。高水平的AFP胃癌被称为产AFP胃癌(AFPGC),目前尚无标准定义,以能检测到AFP的表达(血清水AFP平异常升高,免疫组化AFP阳性)为主要特征和诊断标准。AFPGC的发病率在世界范围内为1.3%-15%3,其具有独特的临床及病理特点,更具侵袭性,更容易发现肝转移、淋巴结转移,预后差4。目前尚缺乏标准治疗方案。
既往研究表明,卡瑞利珠单抗联合阿帕替尼和SOX或卡培他滨和奥沙利铂(CAPOX)后序贯卡瑞利珠单抗和阿帕替尼维持,在胃或胃食管交界处(G/GEJ)腺癌患者中产生了有希望的ORR和PFS结果,并且安全性可耐受5,6。然而,这种联合治疗AFP-GC患者的临床试验数据仍然很少。
该研究旨在评估卡瑞利珠单抗联合阿帕替尼和化疗在未经治疗的AFP-G/GEJ腺癌(AFP-G/GEJ)患者中的抗肿瘤活性、安全性和预测性生物标志物。
02研究方法
本研究是一项单臂、II期、多中心临床试验(NCT04609176),旨在评估卡瑞利珠单抗联合阿帕替尼和SOX一线治疗产甲胎蛋白胃/胃食管结合部腺癌患者的抗肿瘤活性、安全性及生物标志物变化。主要终点是基于RECIST v1.1确认的ORR。次要终点包括DCR、PFS、OS、缓解持续时间、缓解时间及安全性等。
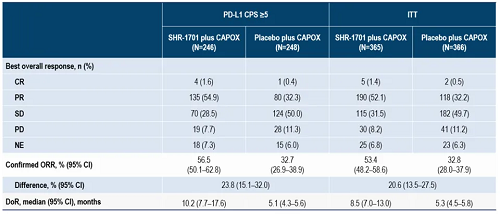
图1. CAP 06研究设计
03研究结果
1基线及受试者分布
2020年12月4日至2023年8月4日期间,研究共纳入36例患者。其中30例患者(83.3%)为男性。大多数患者临床分期为IVB期(n=31,86.1%)。18例患者(50.0%)伴有肝转移,17例(47.2%)伴有远处淋巴结转移,9例(25.0%)伴有腹膜转移。中位血清AFP水平为739.8ng/ml(范围:77.7-321847.0)。

表1. 患者基线情况
所有患者均接受治疗。10例患者提前终止治疗。26例患者(72.2%)完成4周期卡瑞利珠单抗联合阿帕替尼和SOX治疗后,仍继续接受卡瑞利珠单抗联合阿帕替尼维持治疗。截至数据截止日期,23例患者终止治疗,其中疾病进展15例,主动退出4例,接受新抗肿瘤治疗2例,另有2例患者因治疗效果好转手术。
2临床疗效
36例患者接受治疗并进行肿瘤疗评评估,2例患者达到完全缓解(CR),22例达到部分缓解(PR),确认的ORR为66.7%(95% CI:49.0-81.4)。DCR为88.9%(95% CI:73.9-96.9)。mDoR为8.4个月,至缓解时间(TTR)为1.4个月。
截至数据截止日期,中位随访时长为11.7个月(范围:3.2-37.9)。共发生23个PFS事件和17个OS事件。中位PFS为7.8个月(95% CI:4.9-12.3)。9个月和12个月PFS率分别为39.2%、35.3%。中位OS为18.0个月(95% CI:10.5-NR)。9个月和12个月OS率分别为76.7%、67.0%。
3安全性分析
未发生因TRAE导致终止治疗。大多数TRAE安全可控,研究未发现新的安全信号。
4探索性分析
基因测序结果显示,AFPGC最常见的体细胞改变是TP53突变(80%),其次是MCL1(32%)、CCNE1(24%)和ZNF217(24%)。与TCGA数据相比,AFPGC中TP53突变率显著更高,而ARID1A突变率显著降低。我们发现,LRP1B基因突变和PI3K通路改变仅出现在无持久获益(NDB)组,提示与NDB(较差的PFS)显著相关。肿瘤突变负荷(TMB)、拷贝数变异(CNV)负荷与临床疗效之间无关联。

图2. 探索性研究概要(a)及研究队列的基因组特征(b)
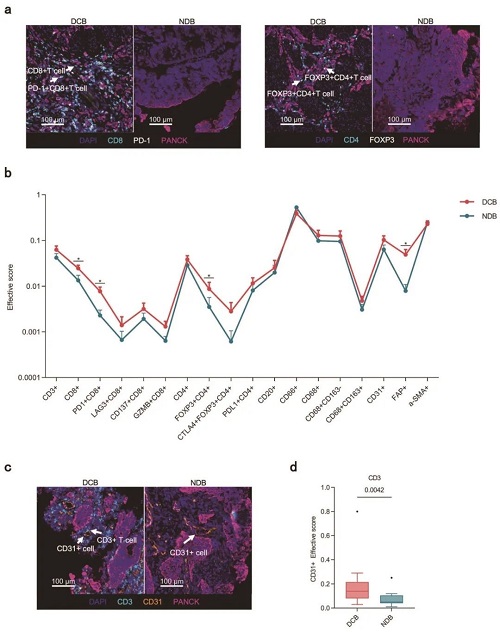
在免疫微环境分析中,发现持久临床获益(DCB)组患者具有更高的CD3+T、CD4+ T和CD8+ T细胞密度。特别是PD-1+CD8+ T细胞、PD-L1+CD4+ T细胞和CD4+FOXP3+CTLA4+ T细胞在DCB组中显著富集。同时高表达FOXP3+CD4+和PD-1+CD8+细胞的患者获益比例更高(83.3% vs 45.0%)。

图3. DCB组和NDB组的肿瘤浸润细胞总体景观和密度比较
治疗前后比较显示,经抗血管生成药物阿帕替尼联合卡瑞利珠单抗治疗后,通过促进血管正常化和内皮细胞活化,CD3+ T细胞和CD8+ T细胞密度显著增加,表明该联合方案能募集T细胞,将“冷”微环境转变为更“热”的炎症微环境,可能是其取得良好疗效的重要机制。

图4. AFP-G/GEJ腺癌的空间分析显示肿瘤浸润细胞
在不同治疗效果下存在组织层次
04研究结论
卡瑞利珠单抗联合阿帕替尼和SOX序贯卡瑞利珠单抗联合阿帕替尼一线治疗产甲胎蛋白胃或胃食管结合部腺癌显示出良好的抗肿瘤活性和安全性。探索性分析揭示了产AFP胃癌独特的分子和免疫特征,还为预测治疗反应提供了潜在生物标志物。
参考文献:
1.Wang, Y., Lu, J., Chong, X. et al. PD-1 antibody camrelizumab plus apatinib and SOX as first-line treatment in patients with AFP-producing gastric or gastro-esophageal junction adenocarcinoma (CAP 06): a multi-center, single-arm, phase 2 trial. Sig Transduct Target Ther 10, 100 (2025). https://doi.org/10.1038/s41392-025-02193-z
2.Wang Y, Wang C, Chen X, et al. Camrelizumab plus apatinib and SOX as first-line treatment in patients with alpha-fetoprotein–producing gastric or gastroesophageal junction adenocarcinoma: A single-arm, multi-center, phase 2 trial[J]. Journal of Clinical Oncology. Volume 42, Number 3_suppl. 2024 ASCO GI poster 351.
3.Chun H, Kwon SJ. Clinicopathological characteristics of alpha-fetoprotein-producing gastric cancer. J Gastric Cancer. 2011;11(1):23-30. doi:10.5230/jgc.2011.11.1.23
4.Sun W, Liu Y, Shou D, et al. AFP (alpha fetoprotein): who are you in gastrology?. Cancer Lett. 2015;357(1):43-46. doi:10.1016/j.canlet.2014.11.018
5.Peng, Z. et al. Camrelizumab combined with chemotherapy followed by camrelizumab plus apatinib as first-line therapy for advanced gastric or gastroesophageal junction adenocarcinoma. Clin. Cancer Res. 27, 3069–3078 (2021).
6.Chen, X. et al. First-line camrelizumab (a PD-1 inhibitor) plus apatinib (an VEGFR-2 inhibitor) and chemotherapy for advanced gastric cancer (SPACE): a phase 1 study. Signal Transduct. Target Ther. 9, 73 (2024).
300多万优质简历
17年行业积淀
2万多家合作名企业

微信扫一扫 使用小程序

